Le diagramme de Mollier

Le diagramme de Mollier est une représentation graphique de la relation entre la température de l'air, la teneur en humidité et l'enthalpie.
Il sert également d'outil de conception de base pour les travailleurs de la construction et les ingénieurs. En termes d'entropie et d'enthalpie, le diagramme des propriétés thermodynamiques d'une substance est constant.
Origine du diagramme de Mollier
Richard Mollier (1863-1935) a passé la majeure partie de sa vie professionnelle à étudier les propriétés des milieux thermodynamiques et leur représentation efficace sous forme de graphiques et diagrammes, à la Technische Hochschule de Dresde. La vulgarisation de l'utilisation de l'enthalpie est au cœur de ses recherches. En 1904, le chercheur a conçu la première carte de l'enthalpyentropie. Puis il a publié d'autres variétés de cartes basées sur l'enthalpie. Ainsi, en 1923, le Bureau des normes des États-Unis a reconnu son travail et l'a nommé diagrammes de Mollier.
L’enthalpie c’est quoi ?
L'enthalpie détermine la fonction de l'état dont la valeur dépend uniquement de l'état initial et final du système. La première étape de la thermodynamique consiste à mesurer la chaleur de diverses réactions. L'objectif principal de la thermodynamique est basé sur la loi de la conservation d'énergie, c'est-à-dire mesurer l'enthalpie et/ou la chaleur des différents processus chimiques. En effet, chaque processus chimique est associé à une enthalpie.
La réaction exige une pression constante face à un changement d'enthalpie. Les valeurs absolues des énergies internes sont basées sur un état standard, comparable à une quantité donnée. Les états standard actuels sont liquides, gaz et solide.
Et l’entropie ?
L'entropie est la mesure du désordre d'un système thermodynamique, c'est-à-dire que sa valeur varie en fonction de la quantité de matière présente. La lettre "S" fait référence à l'entropie dans les équations et les unités de joules par kelvin (J?K-1) ou kg?m2?s-2?K-1. Seul un système très ordonné a une faible entropie.
L'entropie de l'univers pourrait augmenter si le système fonctionne mal selon certains scientifiques. L'énergie thermique pourrait libérer une grande quantité de chaleur qui pourrait éventuellement mener à l'extinction de l'univers. Cependant, d'autres scientifiques contestent cette théorie. Certains comparent l'univers à un système et admettent que les deux sont également sensibles à la mesure de l'entropie. Alors que d'autres considèrent l'univers comme faisant partie d'un vaste système.
Les types d’enthalpie
Il existe différents types d'enthalpie de réaction, observés en chimie des sels fondus, comme :
- L'énergie de liaison,
- L'enthalpie de mélange,
- L'enthalpie de dissolution,
- L'enthalpie de transformation polymorphique.
L'enthalpie de fusion est considérée comme fiable en présence de composés binaires et de mélanges eutectiques. Cette fiabilité dépend du choix des conditions de simplification, des informations reçues, de la différence entre les points de fusion des composants et des composés binaires, des températures eutectiques.
Le diagramme enthalpique de Mollier
Le diagramme Mollier H-S (Enthalpie v Entropie) converge avec le diagramme T-S (Température v Entropie) proposé par Gibbs. Le premier conserve les avantages du second tout en en inventant d'autres. En effet, les diagrammes d'enthalpie représentent l'énergie interne relative à un système, avant et après une réaction. L'énergie du système et sa nature sont démontrées par des lignes horizontales.
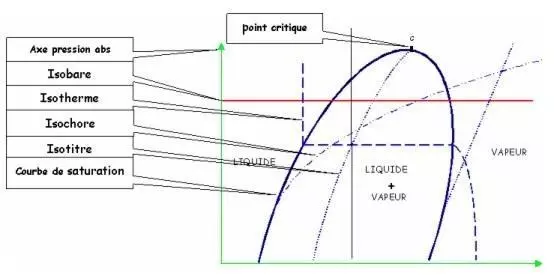
Les formules de tous les éléments ou composés et leurs états, c'est-à-dire solide, liquide, gazeux, sont présents dans le système. L'axe « y » n'a pas d'échelle car l'enthalpie ne peut pas être mesurée. Le changement physique ou chimique de l'enthalpie du système est représenté par une ligne. L'axe « x » montre la progression de la réaction.
Quel est l’intérêt de ce diagramme ?
Les lignes verticales qui représentent les processus réversibles et les lignes horizontales qui représentent l'énergie constante sont les principaux avantages de ce diagramme. La présentation synthétique des cycles de production d'énergie et de réfrigération présente d'autres avantages. Avec cette technique, le travail peut être calculé directement à partir de distances verticales, c'est-à-dire par opposition aux zones sur les diagrammes T-S et P-V. De plus, les défaillances du système sont clairement indiquées dans le diagramme H-S.


